在有机合成中,如何在芳香环的多个位点上实现位置单一可控的烷基化反应,一直是个巨大挑战。特别是对于芳基腈这类本身反应性较差的底物,传统方法往往存在区域选择性不可控、需使用强酸或昂贵金属催化剂、反应条件剧烈等问题。针对上述问题,酒店偷拍
章维华和夏青团队开发了一种通过简单更换烷基卤化物即可精准调控芳基腈烷基化反应区域选择性的新策略。近期,该研究工作以“Alkyl halides dictate site selectivity in aromatic nitrile alkylations”为题,发表在国际知名期刊《Chinese Chemical Letters》。

该研究在相同的光催化反应体系中,将烷基溴化物更换为烷基碘化物,即可像“开关”一样,轻松地将反应路径从“氰基位点取代”切换至“碳氢位点烷基化”,从而高选择性地获得两种结构迥异的烷基化产物。这种底物控制的模式,为合成化学家提供了新颖的反应灵活性和精准度。
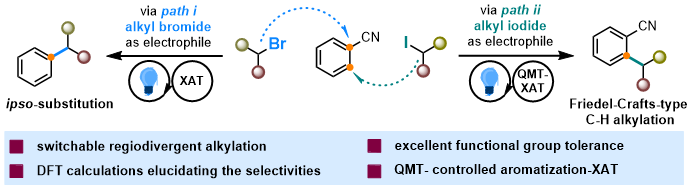
图1烷基卤化物控制芳香腈烷基化反应区域选择性
通过自由基捕获实验、自由基钟实验、荧光猝灭实验、链式反应等验证实验证实了反应为自由基路径,并初步证明烷基溴化物与烷基碘化物分别导向ipso-取代和Friedel-Crafts型C–H烷基化机理。
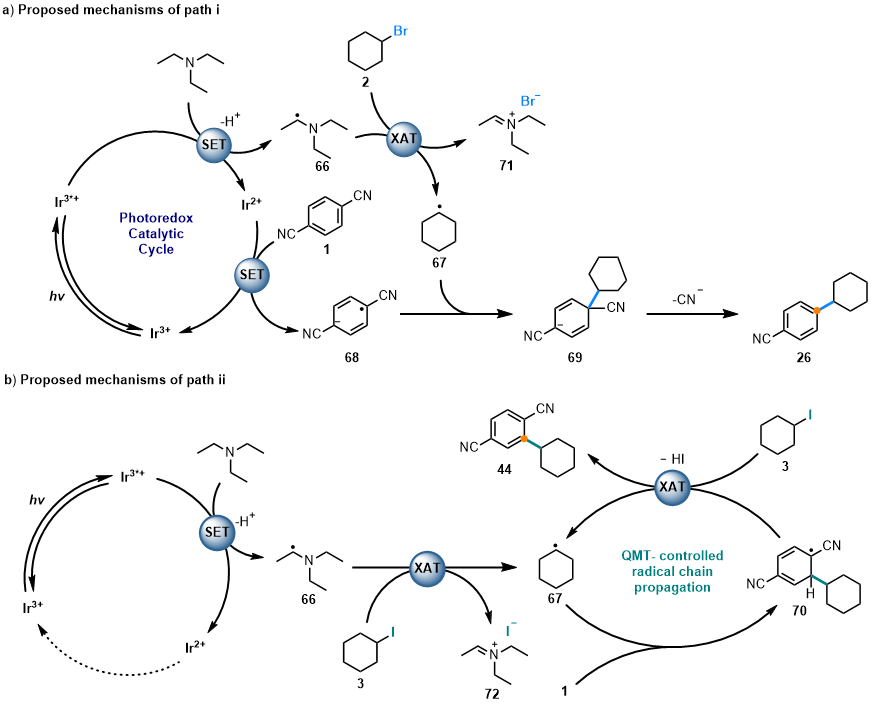
图2可能的反应机理
结合机理探究实验,理论计算进一步揭示了两种路径分岔的根源。ipso-取代路径(path i)经由自由基加成-氰基离去过程。C–H烷基化路径(path ii)则涉及量子力学隧穿效应(Quantum Mechanical Tunneling, QMT)促进的芳构化-卤素原子转移过程,该机制在低温下仍保持高效,进一步验证了隧穿主导的氢转移过程。
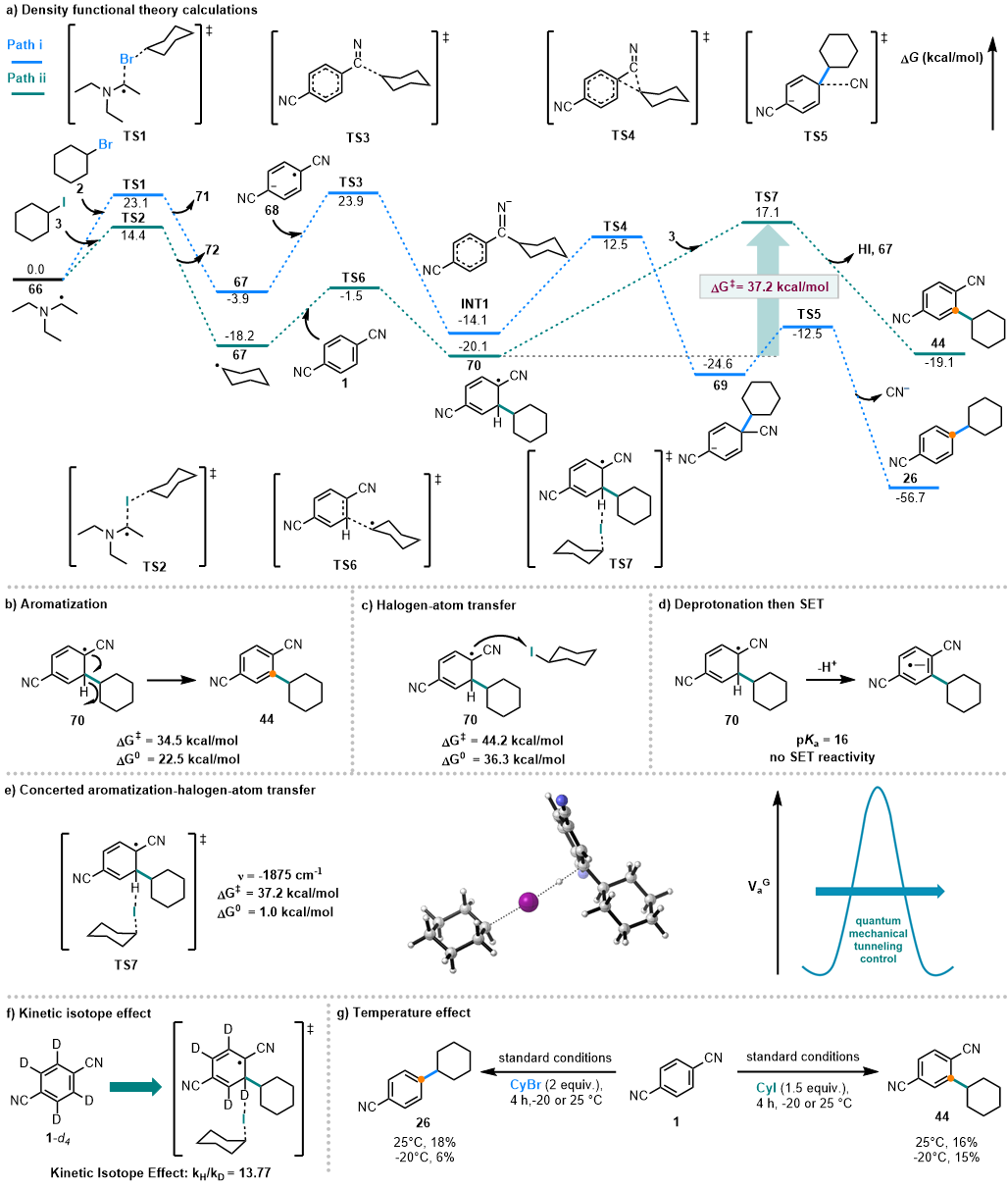
图3 DFT计算(概述可能导致量子隧道控制协调卤素原子转移的机制方案)
该方法适用于多种芳基腈与环状、链状烷基卤化物,兼容酯基、氯代、内酯等重要官能团,并成功应用于天然产物衍生物的后期官能化,展示了良好的应用潜力。这项研究不仅发展了高效实用的合成新方法,更在反应机理的认知上取得了重要进展,为药物研发及功能分子的高效构筑提供了强有力的新工具。
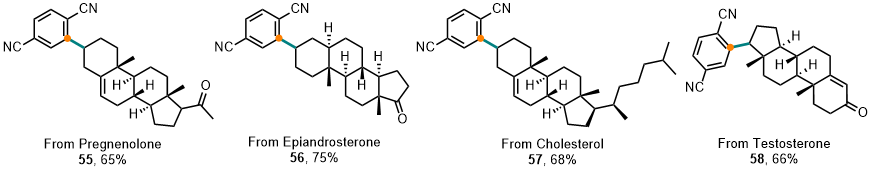
图4天然产物衍生物的后期修饰
酒店偷拍
博士研究生朱宇川为论文第一作者,博士研究生谢凯丽在理论计算部分做了重要贡献,章维华教授和夏青副教授为共同通讯作者。酒店偷拍
博士后李宇飞、刘芳教授、先正达集团首席科学家顾玉诚教授、南开大学汪清民研究员共同参与了该研究。该研究得到了江苏省自然科学基金优秀青年科学基金项目、国家自然科学基金项目、中央高校基本科研业务费等项目资助。
文章链接:://doi.org/10.1016/j.cclet.2025.111819